20個國內特有品種,迎來評價辦法
加入日期:2019/6/25 12:00:19 查看人數: 1268 作者:admin
重磅!20個國內特有品種,迎來評價辦法,不重新開展臨床試驗,國家藥監局將不建議使用。
剛剛,國家藥品監督管理局藥品審評中心發布《國內特有品種評價建議》的通知。

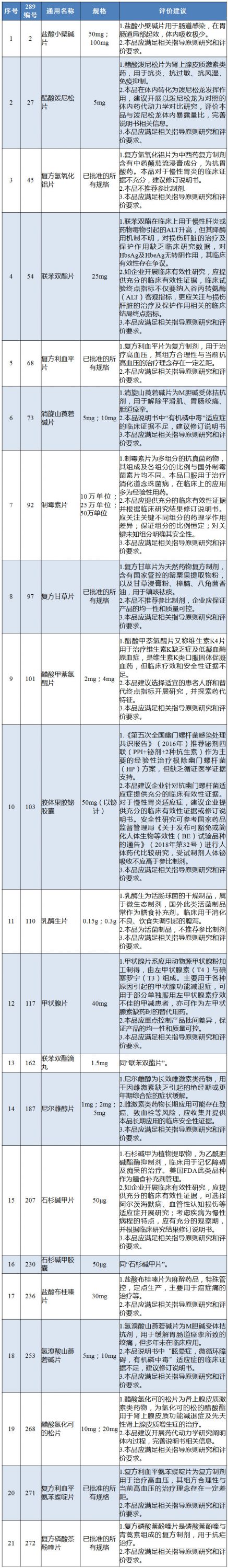
據通知,為落實原總局《關于仿制藥質量和療效一致性評價工作有關事項的公告》(2017年第100號)的要求,仿制藥質量與療效一致性評價辦公室組織人員對《關于落實<國務院辦公廳關于開展仿制藥質量和療效一致性評價的意見>有關事項的公告》(2016年第106號)附件中的國內特有品種進行了梳理調研、專家論證和征求意見,明確了各品種的評價建議,現予發布。
企業應當承擔主體責任,根據原總局發布的《總局關于發布仿制藥質量和療效一致性評價品種分類指導意見的通告》(2017年第49號),同時結合附件中的評價建議及相關技術指導原則,對國內特有品種進行深入研究。

根據原食藥監總局2017年第49號文件的要求,針對國內特有品種,由企業選擇可重新開展臨床試驗證明其安全有效性,并參照《化學藥品仿制藥口服固體制劑質量和療效一致性評價申報資料要求(試行)》提交申請,后續審核通過后視同通過一致性評價。
企業未選擇重新開展臨床試驗的,國家食品藥品監督管理總局對外公布其缺乏有效性數據,不建議使用。
可以看到,一致性評價的進程由易到難,已經從口服劑型、注射劑型,再到國內特有品種了。雖然這些國內特有品種缺少參比制劑,但是仍然需要滿足相關指導原則研究和評價要求。
而這些藥品是否將呈現有效的數據,也將決定他們后續的命運。
附:國內特有品種評價建議